個人的な話から始めます。ボクは大学卒業後医者になり、がん患者さんがたくさん入院している病棟に配置されました。カンファレンスで治療法が決定され、抗がん剤の点滴などを上司に指示され、検査や投薬に走り回ることになります。患者さんによっては、徐々に悪化し亡くなります。患者さんも家族も言葉では表わせない気持ちで祈っている、新人医師も頑張る、しかし負け戦が続いてしまう、、、今回のブログは、TNBC論文を投稿したことをきっかけに、がんについて書いてみます。
癌にもいろいろある
臓器別に、肺がん、胃がん、子宮がん、皮膚がん、と呼ばれますが、各分野において治療法が確立されていないサブタイプがあり、例えば、肺がんの中で10%ほどを占める小細胞癌は、確実な薬が開発されていません。また、乳がんの中で15%はトリプルネガティブ乳がんという「既知のバイオマーカーが通用しない」集団です。すると「効く薬はないし手術もできないので、家かホスピスで有意義に過ごしてください」という流れになります。
なぜ良い薬がないのか?
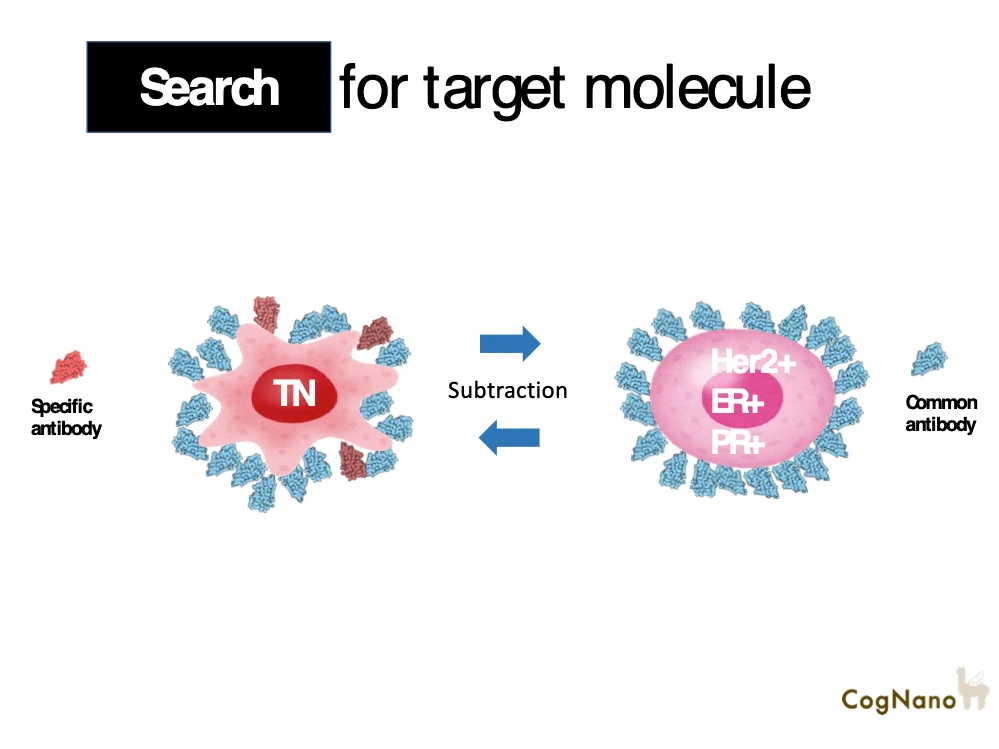
最大の理由は「標的分子がわからない」からです。標的分子がわかりさえすれば、その分子を目印として治療法を開発できます。ここでいう標的分子とは「がん細胞」を健康な細胞と区別するためのバイオマーカーのことを言います。例えば、「がん細胞」だけをマークする抗体を開発し、抗がん剤を付けて点滴すれば、標的細胞だけを消滅させることができます。しかし、標的分子を知らなければ、創薬を開始することすらできません。人間にとって最も苦手なのは、「存在するかどうかわからないものを見つける」ことです。膨大な努力と資金を投入して探索しても存在しないかもしれない。これまで「標的分子を探索する」役割はアカデミアに委ねられてきましたが、分子医学研究者は「自分にとって興味がある細胞や分子にフォーカス」する傾向があり、網羅的なサーベイをすることは難しい構造があります。なぜなら、特定の分子や細胞を突き詰めて研究をすることが、専門家として、とり急ぎ学会での成果とみなされる傾向があるからです。製薬会社は大学から良い情報が出てくるのを待っており、研究者は自分の興味に従って研究している。残念ですが、そこに期待と現実の谷間があります。
2番目の理由は、経済的な要請です。がんによっては治療法が確立し、救命率(5年生存率)が上がっています。標的分子がわからないようながんは、次第にマイナーなカテゴリーになってきています。すると、開発コストの割に市場規模が小さく、大きなリターンを期待できない。売上1千億円以上を見込めないと創薬を開始できない経済構造があり、製薬会社が開発を躊躇する理由になります。日本で年間千人程度なら少数とされますが、患者さんからみれば、数が少ないという理由で放っておかれるのは理不尽でもあります。
分子標的創薬~Unmet Medical Needsとは
前置きが長くてすいません。この40年間、標的分子を探す努力が実を結び、Her2, EGFR, PD-1L, OX40などの画期的な創薬標的分子が見つかってきました。今では、創薬エンジニアリングである「ADC: antibody-drug-conjugate」「CAR-T」などが花開き、驚異的な売上を示すブロックバスターの多くは「分子標的医薬」です。つまり、標的分子を目印として効果を発揮する抗体系医薬です。そういえば昔よりも、がんは治りうる病気、死なない病気、という印象が強くなってきました。これは分子標的医薬の貢献が大きいといえます。一方依然として、あっという間に進行するがんもあり、時折、膵がんや胆管がんなどが原因で、まだ若い俳優・女優が亡くなったというニュースが流れます。それらは、良く効く薬がないカテゴリーで、専門用語でUnmet Medical Needsと呼ばれます。
データから標的を発見できないものか?
誰も知らない標的分子を探すCOGNANOの作業は、探検家が探し尽くした後に財宝を掘り出すようなプロジェクトです。非情にも、財宝は存在していないかもしれません。ボクたちの体の中にはタンパク質だけで(控えめに言って)数十万種類の分子が発現しています。このスケールで「がん細胞」だけに存在する(かもしれない)標的分子をサーチできるシステムは、生物の抗体免疫システムしか存在していません。生物の抗体遺伝子ハイパーミューテーション(超変異)による巨大な計算能力は、今の所、in vitroでもin silicoでも再現できません。問題はこの情報をヒトが解読できるかにかかっています。

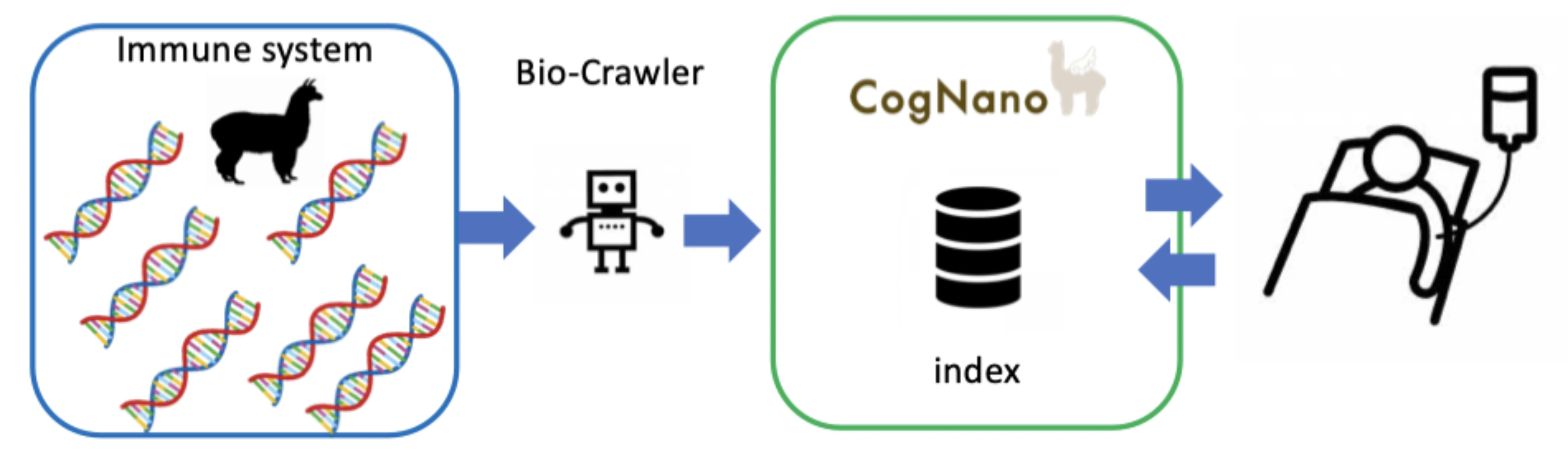
魚群探知機をイメージして下さい。腕の良い漁師、素晴らしい漁船がある場合、獲物の所在がわかれば、成功効率は上がるはずです。全海洋面を探査するレーダーが抗体免疫システムであり、自然が与えてくれる巨大なデータセットをヒトに分かるように翻訳するのが、COGNANOのITチームというわけです。初期のCOGNANOはバイオ情報から数理解析するまでに何年もかかりましたが、今ではITチームに送れば最適解を返答してくれるまでに成長しました。今回、トリプルネガティブ乳がんのバイオマーカー発見を例として、技術のあらましを公開します。
COGNANOは、希少がんを含めたUnmet Medical Needsを解決するため、抗体遺伝子情報をデータベースにして高速に打ち出していきます。この成果を製薬業界に託し、一刻も早く、取り残されている患者さんのベッドサイドに届くことを期待しています。

ふり返り、はまだ早い
30年前に手も足も出なかった自分ですが、気づけば、アルパカが第一計算機、解析プログラムが第二計算機であり、答えが出てくるのを待っているだけの管理人になっていました。こんな展開が待っているとは思いませんでしたが、自分の知能で理解する範囲を超えていることは納得しています。患者さんに届けるためには別の戦い、つまり資本・許認可を含めて長い道のりであり、タソガレている余裕はありません。COGNANOだけでは乗り越えられない壁がそびえています。患者さんや製薬関係者様を含め、みなさまのご声援とご賛同をお待ちするしかありません。では、わたしたちの論文をお楽しみください、、、